Lần đầu tiên kể từ khi TPD (Translucent post-larvae disease: Bệnh mờ đục ở tôm giống) bùng phát trên quy mô lớn vào năm 2020, cơ chế gây bệnh cực kỳ nguy hiểm của vi khuẩn gây bệnh V TPD được tiết lộ. Một chủng Vibrio parahaemolyticus có độc lực cao (Vp -JS20200428004-2) đã được xác định là mầm bệnh gây ra bệnh TPD truyền nhiễm và được đặt tên là Vibrio parahaemolyticus gây bệnh TPD, hoặc Vp TPD.
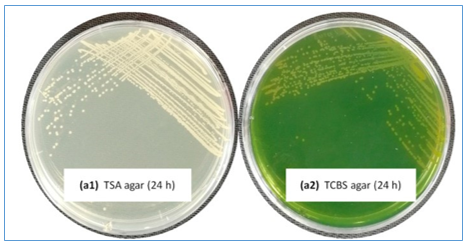
Hình 1: Khuẩn lạc vi khuẩn JS20200428004-2 cho thấy màu trắng sữa trên môi trường thạch TSA với cạnh gọn gàng và bề mặt nổi, đường kính là 1,79 mm sau khi ủ trong 24 giờ ở 28 °C; tuy nhiên, khuẩn lạc có màu vàng nhạt trên môi trường thạch TCBS và đường kính là 2,04 mm sau khi ủ trong 24 giờ ở 28°C
TPD chủ yếu xảy ra ở tôm thẻ giống giai đoạn 4 – 7 ngày tuổi (postlarvae: PL) PL4~P7, bệnh lây lan nhanh, tỷ lệ mắc bệnh có thể lên tới 60% vào ngày thứ hai sau lần đầu tiên quan sát thấy những cá thể bất thường, và thậm chí lên tới 90–100% trong những trường hợp nặng vào ngày thứ ba. Và mức độ lây nhiễm rất nặng, tỷ lệ tử vong cao, tỷ lệ tử vong của tôm giống đạt 100% sau 3 ngày kể từ khi phát bệnh.
Tôm giống nhiễm bệnh mờ đục (TPD) có các dấu hiệu lâm sàng như: gan tụy và đường tiêu hóa bất thường các tế bào biểu mô gan tụy và ruột bị hoại tử và bong tróc (dưới kính hiển vi), gan tụy nhợt nhạt hoặc không màu và đường tiêu hóa trống rỗng, khiến tôm giống trở nên trong suốt và mờ đục; được đặt tên là “tôm giống mờ đục: TPD: translucent post-larvae” hoặc “tôm giống thủy tinh: GPD: glass post-larvae”.

Năm 2023 bệnh TPD phổ biến nên người nuôi dùng diệt khuẩn thậm chí dùng kháng sinh để ức chế hoặc diệt khuẩn, do nhu cầu sản xuất tôm không kháng sinh đã thúc đẩy sự ưu tiên cao của các biện pháp an toàn sinh học, bao gồm phát hiện sớm và điều trị khử trùng để ngăn chặn sự xuất hiện và phổ biến của TPD. Vì thế, nhu cầu cấp thiết là phải điều tra yếu tố độc lực chính của Vp TPD, phát triển kỹ thuật chẩn đoán hiệu quả và các chiến lược phòng ngừa TPD.
Nghiên cứu các yếu tố hoạt động của Vp TPD bằng cách phân tích hai protein độc lực của Vp TPD_ 4-2-1 và Vp TPD_ 4-2-2 được mã hóa bởi GE005140 và GE005139 trong Vp TPD, Vibrio protein độc lực cao (Vibrio high virulent protein: VHVP-1 (GE005140: vhvp-1) và (VHVP-2 (GE005139: vhvp-2)), được xác định là yếu tố độc lực chính gây ra TPD. Hơn thế nữa, VHVP-1 và VHVP-2 được phát hiện nằm song song trên một plasmid có kích thước 187.791-bp của bộ gen Vp TPD. Điều tra dịch tễ học sâu hơn chỉ ra rằng chủng V. parahaemolyticus chỉ mang gen vhvp-1 và thiếu gen vhvp-2 không thể gây chết tôm thẻ Penaeus vannamei, V. parahaemolysiscus gây chết tôm giống bằng cách thu được yếu tố độc lực VHVP-2. Các đoạn protein được tạo thành có trọng lượng phân tử khác nhau (MWs) từ Vp TPD, và thấy rằng những đoạn protein có MW>100 kDa mới có khả năng gây chết tôm sau 16 giờ thử nghiệm và đạt tỷ lệ tử vong 90% sau 32 giờ thử nghiệm. Nghiên cứu làm sáng tỏ hơn về cơ chế gây bệnh của VpTPD và phát triển các chiến lược chẩn đoán sớm bệnh TPD ở trại giống tôm.
Phân tích mô bệnh học của các mẫu từ các nhóm nghiệm khác nhau.
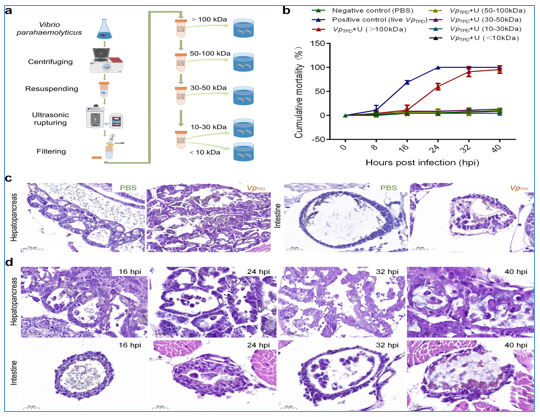
Hình 3: Phân tích khả năng gây bệnh của protein Vp TPD có trọng lượng phân tử khác nhau đối với Penaeus vannamei hậu ấu trùng.
(a) Sơ đồ các giao thức được sử dụng để thu được Protein Vp TPD có trọng lượng phân tử khác nhau.
(b) Tỷ lệ tử vong tích lũy của P. vannamei sau ấu trùng được tạo ra bởi các trọng lượng phân tử khác nhau của Vp Protein TPD trong thử nghiệm.
(c) Mô bệnh học: Hình ảnh gan tụy và ruột của P. vannamei post từ nhóm bị thử nghiệm bởi Vp TPD.
(d) Hình ảnh mô bệnh học của gan tụy và ruột của P. vannamei post từ nhóm thử nghiệm Vp TPD + U (>100 kDa) tại các thời điểm khác nhau sau gây nhiễm (bao gồm 8 hpi, 16 hpi, 24 hpi, 32 hpi và 40 hpi).

Hình 4: Bản đồ bộ gen và plamid hình tròn của nhiễm sắc thể Vp TPD và Vp 1616 và cấu trúc miền của gen vhvp-1 và vhvp-2 của Vp TPD.
(a) Bản đồ bộ gen hình tròn của nhiễm sắc thể số 1 và nhiễm sắc thể 2 của Vp TPD.
(b) Bản đồ bộ gen của nhiễm sắc thể 1 và nhiễm sắc thể 2 của Vp 1616.
(c) Bản đồ hình tròn của plasmid 1, plasmid 2 và plasmid 3 của Vp TPD.
(d) Bản đồ bộ gen của plasmid 2 (187.791 bp) của Vp TPD.
(e) Cấu trúc của các protein được mã hóa bởi vhvp-1 và vhvp-2 trong plasmid 2.
Phát hiện Vp TPD bằng PCR
Để phát triển phương pháp phát hiện PCR đối với Vp TPD, mồi PCR được thiết kế
để nhắm mục tiêu các gen vhvp-1 và vhvp-2. Cả hai mẫu DNA từ Vp TPD phân lập và mô tôm bị TPD có thể được nhân rộng và sản xuất. Bộ khuếch đại 362, 351 và 303 bp sử dụng Vp TPD – vhvp-1 -F1/R1, Vp TPD – vhvp-2 -F1/R1, và bộ mồi Vp TPD – vhvp-2 -F2/ R2 tương ứng (Hình 4a).
Phân tích độ đặc hiệu của mồi được thực hiện bằng cách sử dụng các mẫu DNA từ các chủng non-VpTPD. Các kết quả cho thấy không có sản phẩm PCR dự kiến nào được khuếch đại khi sử dụng DNA từ mẫu non-VpTPD, điều này chỉ ra rằng các bộ mồi PCR chỉ có tính đặc hiệu đối với Vp TPD (Hình 4b)

Hình 5: Sơ đồ vị trí của mồi PCR của các gen yếu tố độc lực Vp TPD và phân tích dịch tễ học phân tử dựa trên gen vhvp của Vp TPD.
(a) Sơ đồ của gen yếu tố độc lực Vp TPD (vhvp) vhvp-1 và vhvp-2 và các đoạn mồi phát hiện nhắm vào các gen vhvp.
(b) Điện di phát hiện phân tử của các gen vhvp mã hóa miền bảo tồn của TcdA trong gen vhvp-1, SpvB và TcdB trong gen vhvp-2 ở các mầm bệnh khác. Lane 1 Vp TPD; lane 2 Vibrio parahaemolyticus -0421B; lane 3 Pseudoalteromonas (CDM8); lane 4 Vibrio parahaemolyticus gây AHPND (20200610006-16); lane 5 Vibrio alginolyticus
(20150606001-2); lane 6 Vibrio harveyi (20170902102-3); lane7 Vibrio Owensii (20150709001-2); lane 8 Vibrio campbellii (20150606027-2); lane M phân tử điểm đánh dấu trọng lượng (bp).
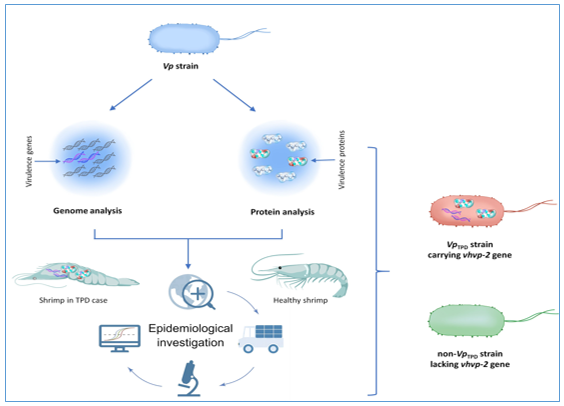
Hình 6: Sơ đồ các quy trình được sử dụng để xác định yếu tố độc lực chính của Vp TPD
Nguồn:
- Determination of the infectious agent of translucent post-larva disease (TPD) in Penaeus vannamei. Pathogens, 9(9), 741. Được nghiên cứu bởi Ying Zou & cs. (2020)
- Tạp chí Microbiology Spectrum, https://www.researchgate.net/publication/374827157_Vibrio_parahaemolyticus_becomes_lethal_to_post-larvae_shrimp_via_acquiring_novel_virulence_factors.
Nhãn
Tin tức liên quan
01 tháng 07 2025
Giấy phép môi trường năm 2025 – Nhà máy Đồng Nai
19 tháng 05 2025
📢 HUẤN LUYỆN AN TOÀN VỆ SINH LAO ĐỘNG – AN TOÀN LÀ SỐ 1 📢
19 tháng 05 2025
✨ FOUNDATION LEADERSHIP 2025 – NEW START, NEW STAR ✨
03 tháng 05 2025






















